- 사노피 개발 젠포자임, 현존하는 유일한 ASMD 치료제
- “규제 과학 기반해 치료제가 신속하게 공급될 수 있도록 최선”
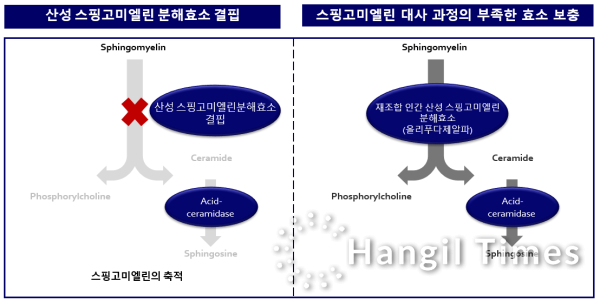 젠포자임주 작용기전 설명 자료/제공 식품의약품안전처[이승준 기자] 식품의약품안전처(식약처)는 프랑스 빅파마 사노피가 개발한 희귀의약품 ‘젠포자임주’(성분명 올리푸다제알파)를 허가했다고 25일 밝혔다. 젠포자임주는 산성 스핑고미엘린 분해 효소 결핍증(ASMD.acid sphingomyelinase deficiency) 치료에 사용된다. 사노피-아벤티스코리아가 수입한다.
젠포자임주 작용기전 설명 자료/제공 식품의약품안전처[이승준 기자] 식품의약품안전처(식약처)는 프랑스 빅파마 사노피가 개발한 희귀의약품 ‘젠포자임주’(성분명 올리푸다제알파)를 허가했다고 25일 밝혔다. 젠포자임주는 산성 스핑고미엘린 분해 효소 결핍증(ASMD.acid sphingomyelinase deficiency) 치료에 사용된다. 사노피-아벤티스코리아가 수입한다.
ASMD는 산성 스핑고미엘린분해효소의 활성 감소로 비장.간.폐.골수.림프샘 등에 스핑고미엘린이 축적되는 희귀질환이다. 간장.비장의 비대와 폐 질환 등이 나타난다. 환자의 3분의 2 수준이 어린이라 ‘소아성 치매’라고도 불리기도 한다.
이 질환이 있는 소아 중환자들은 신경계 이상으로 만 3세가 되기 전에 사망하는 사례가 많다. 만 3세를 넘기더라도 성인이 되기 전 호흡 곤란을 겪어 생존하는 사례가 거의 없다. ASMD는 25만명 가운데 한 명 정도로 발병하는 것으로 알려졌다.
‘젠포자임주’는 유전자재조합 기술로 제조한 산성 스핑고미엘린 인공 분해 효소다. 현존하는 유일한 ASMD 치료제다. 젠포자임주를 환자에게 투여했을 때 장기 내 스핑고미엘린 축적을 감소, 증상을 완화하는 효과가 있다. 국내에 앞서 일본에서 지난 2022년 3월 허가를 받았다. 유럽(2022년 7월).미국(2022년 9월) 승인도 차례로 획득했다.
식약처 측은 “앞으로도 규제 과학을 기반으로 안전성.효과성이 충분히 확인된 치료제가 신속하게 공급될 수 있도록 최선을 다하겠다”고 전했다.
[궁궐이야기 61] 창덕궁 '금천교' [이승준 기자] 궁궐에는 반드시 금천이라는 냇물이 흐르도록 되어 있다. 경복궁에는 흥례문과 근정문 사이를 가로지르는 인공적인 물길을 만들었지만, 창덕궁의 금천은 북악산 줄기의 매봉에서 돈화문 쪽으로 흘러내리는 자연계류이고, 장대석으로 호안석축을 둘러 궁궐답게 말끔히 정돈했다. 하지만 현재는 물길이 바뀌고 지하수가 고갈...

 서울 편의점 900곳, 배달.퀵 이동노동자에 쉼터 제공
서울 편의점 900곳, 배달.퀵 이동노동자에 쉼터 제공
 산업재해 비용 하도급업체에 전가...공정위, 대한조선 제재
산업재해 비용 하도급업체에 전가...공정위, 대한조선 제재
 상공회의소, 중소.중견기업에 재생에너지 활용 컨설팅
상공회의소, 중소.중견기업에 재생에너지 활용 컨설팅
 법원, 공직자 검증 민간 자격시험 불승인한 정부..."결정 정당"
법원, 공직자 검증 민간 자격시험 불승인한 정부..."결정 정당"
 용인시외국인복지센터, 환경개선 활동으로 지역사회 기여
용인시외국인복지센터, 환경개선 활동으로 지역사회 기여
 한길타임즈 CG
한길타임즈 CG
 신간 '한일 고지도 속의 한반도, 동해 그리고 독도' 발간
신간 '한일 고지도 속의 한반도, 동해 그리고 독도' 발간
 싱어송라이터 고세정, 첫 정규앨범 ‘보통의 용기 A courage from the ordinary’ 발매
싱어송라이터 고세정, 첫 정규앨범 ‘보통의 용기 A courage from the ordinary’ 발매
 김재환에게 3점포 두 방 맞은 문동주, 개인 최다 9실점 강판
김재환에게 3점포 두 방 맞은 문동주, 개인 최다 9실점 강판
 [독지기고] 아직도 영농부산물을 태우고 있습니까?
[독지기고] 아직도 영농부산물을 태우고 있습니까?
 용산가족공원 & 미르폭포
용산가족공원 & 미르폭포

 목록으로
목록으로